Les peptides ( oligopeptides et polypeptides) et les protéines sont costitués de plusieurs acides aminés liés les uns aux autres par des liaisons peptidiques (CO-NH). La structure JMOL permet de se rendre compte de leur propriétés. Comme exemple de peptides simples, on cite la carnosine, l'aspartame et le glucagon.
تعد البروتينات (Protéines) جزيئات كبيرة (Macromolécules) و هي عبارة عن سلسلة أو سلاسل من الأحماض الأمينية (Acides aminés) تتواصل بينها بالروابط البيبتيدية (Liaisons peptidiques). غالبا، نتكلم عن البروتين عندما يتجاوز عدد الأحماض الأمينية 50 حمضا. في حالة أقل من هذا الرقم يسمى الجزيئ بيبتيد (Peptide). كل البر وتينات تحتوي عموما على أربعة عناصر كيميائية و هي الكار بون (Carbone, C)، الهيدروجين (Hydrogène, H)، الأوكسيجين (Oxygène, O) و الأزوت (Azote, N). و بعض البروتينات تضم كذلك الكبريت (Soufre, S) أو الفوسفور (Phosphore, P) أو الإثنين. و يمثل عنصر الأزوت 16% من المكونات
بإمكان الأحماض الأمينية أن ترتبط بعضها بالبعض بروابط كيميائية تساهمية تعرف بالروابط البيبتيدية (Liaisons peptidiques, CO-NH) أو روابط أميد (Liaisons amide) و تجمع مجموعة الكربوكسيل فوق الكاربون
ألفا (α) من الحمض الأول مع مجموعة الأمين فوق الكاربون
α من الحمض الثاني.
المزيد من المعلومات في كتاب علوم الحياة - بيوكيمياء
Avertissement: la visualisation des molecules par JMOL nécessite l'installation de java (https://www.java.com). Si problème activer java pour votre navigateur.
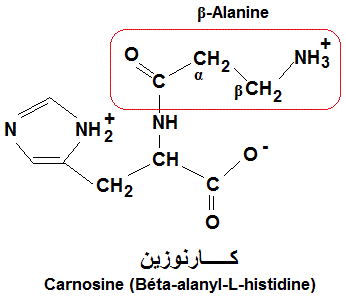
La carnosine (béta-alanyl-L-histidine) est un exemple de dipeptides. Ce peptide spécial est constitué de la béta-alanine
(acides aminé non protéinogène) et de l'Histidine (His) liés entre eux par la liaison peptidique (-CO-NH-).
L'alanine (Ala) est un acide aminé non polaire (apolaire). La béta alanine se disingue par la position du groupement amine sur le carbone béta (carbone
3) au lieu du carbone alpha (carbone 2). His est un acide aminé polaire et essentiel. Les acides aminés peuvent être sélectionnés l'un après l'autre, ainsi que les carbones béta et alpha. La béta-alanine est utilisée par les plantes et les microorganismes dans la synthèse de l'acide pantothénique (vitamine B5), constituant du coenzyme A.
La carnosine, présente dans la viande des mammifère (muscles et cerveau), joue un rôle d'antioxydant
conféré par le groupe imidazole de l'histidine. Elle
fixe les espèces d'oxygène activées, les cations métalliques (Cu++, en particulier) et les radicaux libres. La carnosine est prescrite contre le viellissement. Ce dipeptide n'est pas digéré
complètement, car il contient la béta-alanine (acide aminé anormal avec un groupe NH2 fixé sur le carbone béta
(N° 3) au lieu du carbone alpha ou cabone 2). Son taux élevé
dans les urines rend compte de l'état de l'alimentation carnée
d'origine mammifères.
Il a été décrit qu'un apport complémentaire en
béta-Alanine permet de booster la production de la carnosine
qui fixerait les protons H+ (effet tampon) générés
par l'acidification du muscle ayant subit un exercice intense amenant
à la production d'acide lactique (fermentation). la béta-alanine
augmenterait donc les performances musculaires !
Aspartame: peptide spécial de deux acides aminés (dipeptide): Asp et Phe estétifiée avec un méthyl
L'aspartame, découvert en 1965, est un dipeptide spécial, constitué de l'acide aspartique (Asp) et de la Phénylalanine (Phe) estérifié avec un méthyl (du méthanol) sur le groupe hydroxyle (OH) porté par le carbone 1 (celui du carboxyle COOH). Asp est un acide aminé polaire non essentiel. Phe est un acide aminé non polaire et essentiel.
L'aspartame est un édulcorant à goût sucré (pouvoir sucrant environ 200 fois supérieur à celui du saccharose) utilisé comme additif alimentaire. Son utilisation a été critiquée considérant l'effet qu'il pourrait présenter sur la santé humaine.
Localisez la liaison peptidique dans l'aspartame - حدد الرابطة البيبتيدية في الأسبارتام

L'une des idée pour la production de l'aspartame est de trouver un micro-organisme capable de fournir des quantités substantielles du dipeptide Asp-Phe. Cet objectif peut être atteint en insérant dans le vecteur de clonage un segment d'ADN qui code pour un segment protéique de formule (Asp-Phe)n où n est un grand nombre. Le micro-organisme transformé produira une protéine de taille correspondante avec le segment (Asp-Phe). Après benzylation des groupes carboxyles libres, la protéine est coupée de manière appropriée en segments dipeptides (Asp-Phe), méthylée et débenzylée pour former le peptide Asp-Phe-me (aspartame) qui est utile comme édulcorant.
Sur la base du poids, le métabolisme de l'aspartame génère approximativement 50 % de phénylalanine, 40 % d'acide aspartique et 10 % de méthanol. Des études scientifiques ont montré que l'aspartame est rapidement et complètement dégradé dans l'intestin. L'aspartame n'a jamais été trouvé ni dans le sang ni dans aucun organe après consommation par voie orale.
L'union de deux à une dizaine, environ, d'acides aminés constitue des oligopeprtides. Les peptides contenant entre 30 à 100 acides aminés, environ, sont appelés des polypeptide. plusieurs acides aminés forme un polypeptide. Les protéines sont donc des polypeptides.
L'une des propriétés physiques des peptides et leur état de solides blancs généralement cristalisable et plus ou moins solubles dans l'eau. Leurs point isoélectrique (PI) varient selon la nature des acides aminés qui les composent.
L'une des propriétés chimiques des peptides est la capacité des liaisons peptidiques à former en milieux alcalins, un complexe violet avec les ions cuivriques (réaction de biuret). La réaction de biurée est franchement positive à partir des tétrapeptides(3 liaisons peptidiques CO-NH)
La représentation 'squelette', affiche le peptide sous la forme d'un trait reliant les carbones alpha de chaque acide aminé. Le carbone alpha d'un acide aminé est le carbone 2 en comptant à partir du carbone 1 du carboxyle. Le radical R de l'acide aminé, le groupe carboxyle et amine sont liés au carbone alpha



 |
Contrairement à l'insuline (hormone hypoglycémiante), le glucagon est une hormone hyperglycémiante, de nature peptidique. Elle est sécrétée par les cellules alpha des ilôts de Langerhans. Cette hormone a été découverte pour la première fois en 1923 par Kimball et Murlin |
après des travaux sur des extraits de pancréas. Sa séquence en acides aminés a été déterminée dans les années 1950. Le glucagon est sécrété une fois le niveau du sucre dans le sang diminue.
Etude des liaisons دراسة الروابط
Coloration تلوين
-
Déterminer le nombre d'acides aminés constituant le glucagon Ouvrages de la préparation de la transition Secondaire-Supérieur -
من علوم الحياة إلى البيوكيمياء -
تحميل ملفات في مواضيع البيوكيمياء BIOCHIMIE. TP CONSIGNES (Vidéos) Chaine Youtube (abonnement). Plusieurs vidéos multilingues ANNONCES, INFORMATIONS Congrès, Conférences,... CONCOURS:
- Déterminer les acides aminés N-terminal et C-terminal du glucagon
- Déterminer la séquence complète en acides aminés du glucagon
livre 'Sciences de la vie. Protéines et Enzymes', Baaziz 2013, 306 pages, ISBN : 978-99-54-32-663-3
+ DVD mis à jour + Assistance


- Affiche
- Présentation
du livre
Des Sciences de la vie au Lycée à la Biochimie à l'Université
Téléchargement de fichiers en Biochimie

- Congrès, Conférences
- Cours, Workshops
- Bourses, Postdocs
- Biotech-ecolo annonces
Concours de Pharmacie
Afin de pouvoir continuer à servir les visiteurs, soutenez nos actions sur le site takween en faisant acquisition des ouvrages et supports pédagogiques desitinés à améliorer l'enseignement et la recherche scientfique en Biochimie.