STRUCTURE DES ACIDES AMINES ET PROPRIETES CHIMIQUES. QCM
بنية الأحماض الأمينية
Téléchargement de fichiers en Biochimie SUPPORTS TAKWEEN

La structure des acides aminés (Ac. aminés) - الأحماض الأمينية conditionne leurs propriétés et leurs fonctions biologiques.
| French | Arabic | English |
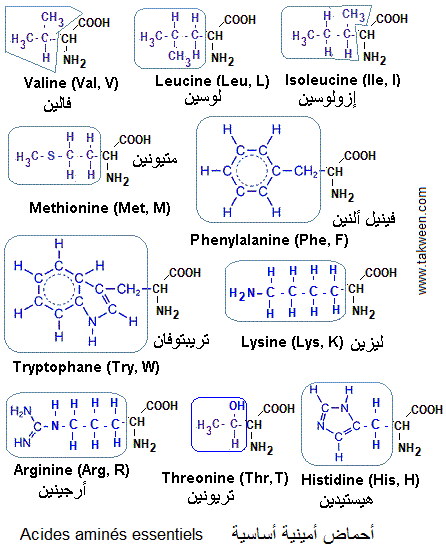
| Acide aminé essentiel, acide aminé indispensable | حمض أميني أساسي | Essential amino acid, indispensable amino acid |
| Ionisation des acide aminés | تأين الأحماض الأمينية | Aminoacid ionisation |
| Chaîne latérale (radical R) des acides aminés | السلسلة الجانبية للأحماض الأمينية | Side chain of amino acids |
Faire les QCM d'abord et regarder plus de détails sur les réponses ensuite.
QUESTION 1. Choisir l'information correcte concernant les Ac. aminés (choisir une seule réponse) (!Le groupement alcool primaire de la sérine et le groupement thiol de la méthionine sont d'excellents nucléophiles)(Les Ac. aminés apolaires interviennent sur la disposition des molécules d'eau dans l'entourage des protéines)(!Le groupement carboxylique de l'acide acétique est 100 fois plus acide que celui de la glycine)(!La proline entraine une grande flexibilité structurale des protéines dans lesquelles elle se trouve)(!Tous les Ac. aminés naturels sont de la série D)
QUESTION 2. Choisir l'information correcte concernant les 20 Ac. aminés:-- cocher une seule réponse - (!Le tryptophane - Trp - présente une absorption minimale à 280 nm)(!Le tryptophane - Trp - présente une absorption maximale à 260 nm)(!Les Ac. aminés Trp, Phe, His et Tyr absorbent tous la lumière dans le proche ultraviolet - 250-300 nm -)(Les Ac. aminés n'absorbent pas la lumière dans le visible)
QUESTION 3. Choisir l'information correcte relative à la glycine (C'est un acide aminé à un pouvoir tampon autour du pH 2,5 et du pH 9,5)(!C'est un acide aminé sans pouvoir tampon car étant neutre)(!C'est un acide aminé à pouvoir tampon autour du pH 2,5 seulement)(!C'est un acide aminé à pouvoir tampon autour du pH 9,5 seulement.)(!C'est un acide aminé à pouvoir tampon autour de son point isoionique)
QUESTION 4. Choisir l'information vraie concernant les Ac. aminés- cocher une seule réponse - (!Certains peuvent posséder plus de deux fonctions acides)(Sont amphotères)(!Présentent tous une absorption dans l'UV à 280.)
QUESTION 5. Choisir l'information correcte à propos de l'histidine- cocher une seule réponse -(!Donne naissance par désamination, à un médiateur impliqué dans l'allérgie)(Acide aminé porteur d'un cycle imidazole)(!Acide aminé à courbe de titration montrant deux pK)(!Acide aminé neutre)
QUESTION 6. Choisir l'information fausse concernant la thréonine - cocher une seule réponse (!Possède un groupement hydroxyle)(!Possède deux carbones asymétriques)(Est un acide aminé non essentiel)
QUESTION 7. C'est un acide aminé possèdant un groupement R à pkR = 6,1 fournissant un pouvoir tampon significatif proche du pH du sang (7,4). Ceci lui permet à pH 7,0 de fonctionner soit comme un catalyseur basique soit comme catalyseur acide et donc jouer un rôle important dans la catalyse enzymatique. De quel acide aminé s'agit-il ?: (!Valine)(Histidine)(!Tryptophane)(!Glycine)(!Sérine)
QUESTION 8. C'est un acide aminé sans carbone asymétrique. Son groupement carboxylique est plus acide que celui de l'acide acétique. Il a un goût sucré. De quel acide aminé s'agit-il ?- cocher une seule réponse - (!Valine)(!Histidine)(!Leucine)(Glycine)(!Sérine)
QUESTION 9. C'est un acide aminé avec groupement alcool primaire considéré comme un excellent nucléophile au cours des réactions enzymatiques et participe à la régulation de certaines enzymes de l'organisme. De quel acide aminé s'agit-il ? :- cocher une seule réponse - (!Valine)(!Histidine)(!Isoleucine)(!Glycine)(Sérine)
QUESTION 10. C'est un acide aminé non essentiel car pouvant être fabriqué à partir de la phénylalanine (parahydoxyphénylalanine). De quel acide aminé s'agit-il ?:- cocher une seule réponse - (!Proline)(!Histidine)(Tyrosine)(!Glycine)(!Sérine)
QUESTION 11. En se basant sur la classification des Ac. aminés selon la polarité, les Ac. aminés Glutamine -Gln-, Tyrosine -Tyr-, Cystéine -Cys-, Thréonine -Thr-, Serine -Ser- et Asparagine -Asn- (retenus par la phrase mnémonique 'Glenn Tire et Cisaille, THéo CERrtifie: c'est un ASsassin') sont:?- cocher une seule réponse -
... Voir détail de la réponse (!Ac. aminés polaires basiques)(Ac. aminés polaires neutres)(!Ac. aminés polaires acides)(!Ac. aminés apolaires)
QUESTION 12 .Choisir l'information correcte relative à la titration de la glycine -
--
Détail de la réponse 12

(!En titrant la glycine par l'acide HCl -courbe 1-, on dissocie les fonctions ionisables -perte de H+- en commençant par la fonction de pK le plus faible -acidité plus grande-)(En titrant la glycine par la base NaOH -courbe 2-, on dissocie les fonctions ionisables -perte de H+- en commençant par la fonction de pK le plus faible -acidité plus grande-)(!En titrant la glycine par la base NaOH -courbe 2-, on sature les fonctions ionisables -gain de H+- en commençant par la fonction de pK le plus élevé -acidité plus faible-)(!En titrant la glycine parl'acide HCl -courbe 1-, on sature les fonctions ionisables -gain de H+- en commençant par la fonction de pK le plus faible -acidité plus élevée-)
REPONSES. DETAILS

Question 1. Les Ac. aminés apolaires sont de nature hydrophobe. Ils s'éloignent de l'eau.
Question 2. Les
Ac. aminés n'absrbent pas la lumière dans le visible
(pas de couleur)
Question 3. La glycine a un pouvoir tampon au niveau de 2,5 et 9,5 ( zones de demi-dissociation
des fonctions carboxyle et amine.
Question 4. Thréonine. Liens: Ionisation de la thréonine, Thréonine: Acide aminé hydroxylé,
Question 5. Histidine. Acide aminé connu par son cycle imidazole.
Question 6. Thréonine = Acide aminé essentiel
Question 7. Histidine (His)
Le corps humain tend à maintenir le pH du milieu extracellulaire à 7,40. Les valeurs physiologiques : 7,36 à 7,42. Les variations maximales compatibles avec la vie : 6,90 à 7,70. Or, il y'a afflux d'acides par l'alimentation et la respiration cellulaire. Les moyens de régulation automatiques sont les systèmes tampons. Le noyau imidazole de l'histidine a un atome d'azote pouvant capter un proton, avec un pKa proche de la neutralité (pKa = 6.1) et des conditions physiologiques. Cette propriété est capitale pour la fonction de certaines protéines comme les enzymes (transfert de protons dans les conditions physiologiques
du cytoplasme (pH proche de 7) et l'hémoglobine pour maintenir
le pH sanguin en agissant comme molécule tampon. Aussi, l'azote
du cycle imidazole de l'histidine peut former des liaisons de coordination
avec des ions métalliques comme Fe2+.
Question 8. Réponse d. Glycine. Le pKa de l'acide acétique (4,75) est plus élevé que le pKa de son dérivé alpha-aminoacide, la glycine. Cette différence de pK de la même
fonction est due au groupe NH3+ qui répulse les protons de COOH.
 |
 |  |
REPONSES. DETAILS (suite)
Question 9. Sérine. Liens:Sérine: Acide aminé hydroxylé,
Question 10. Tyrosine. Liens: Tyrosine: Ionisation, Tyrosine. Acide aminé cyclique
Question 11. Les Ac. aminés Glutamine (Gln), Tyrosine (Tyr), Cystéine (Cys), Thréonine (Thr), Serine
(Ser) et Asparagine (Asn) sont des AA polaires neutres qu'on peut retenir par la phrase mnémonique
'Glenn (Gln) Tire (Tyr) et Cisaille (Cys), THéo (Thr) CERrtifie (Ser): c'est un ASsassin (Asn)'
Question 12. En titrant la glycine par la base NaOH (courbe 2), on va dissocier
les fonctions ionisables (perte de H+) en commençant par la fonction à pK le plus faible (acidité plus grande; COOH sur C alpha). Il est préférable de partir d'un acide aminé complètement saturé avec des protons (ajout avant le départ de la titration, d'un volume faible d'un acide concentré dans la solution d'acide aminé pour avoir
un acide aminé acidifié).
Aussi, on peut faire la titration de la glycine par un acide comme HCl, mais il s'agit cette fois, de saturer progressivement (par les H+ d'un acide) les groupes ionisables en commençant par celui à pK le plus élevé (ici -NH2 sur C alpha pour la glycine). Dans ce cas, il est préférable de partir d'un acide aminé complètement dissocié
(sans protons labiles) obtenu par ajout avant le départ de la titration, d'une base concentrée dans la solution de l'acide aminé donnant ainsi un acide aminé basifié) --- revenir à la question 12.
معايرة الأحماض الأمينية تتم بطريقتين مختلفتين، الأولى تتجلى في تفكيك المجموعات المتأينة تدريجيا (نزع H+) انطلاقا من نقطة pK الصغيرة، (pK COOH, C alpha) ويتم ذلك بإضافة قاعدة مثل NaOH و يحبد الانطلاق من حمض أميني مشبع تماما بالبروتونات (مضاف إليه قليل من حمض) لتكون المعايرة شاملة. أما الطريقة الثانية، فتكمن في تشبيع المجموعات المتأينة بالبروتونات انطلاقاهذه المرة، من المجموعة ذات نقطة pK الكبيرة و يتم ذلك بالإضافة التدريجية لحمض مثل HCl و يحبد الانطلاق من من حمض أميني مفكك تماما (مضاف إليه قليل من قاعدة)
تقويم ذاتي مع التوقيت و التنقيط
Contrôle d'autoévaluation, temporisé, noté et commenté

- Biochimie structurale (Contrôle final QCM corrigé, S3 (archives 2024)
- Contrôle final corrigé du module 'Biochimie structurale', S3 (Archives 2021)
- Contrôle final corrigé des travaux pratique (TP) de Biochimie structurale, S3 (Archives 2021)
- Examen Contrôle corrigé de Biochimie structurale, S3 (Archives 2000)
- Amino acids. QCM on the structure
- Dissociation des acides aminés et espèces chimiques (Exercice)
- Acides aminés. Exercices
- Acides aminés. Ionisation (Exercices)
- Protéines, peptides (contrôles)
- Acides aminés à chaîne hydrocarbonnée
- Acides aminés hydroxylés
- Acides aminés soufrés
- Acides aminés basiques
- Acides aminés dicarboxyliques
- Acides aminés cycliques
- Ionisation des acides aminés, texte Ar
- Peptides,
protéines. Exercices
- QCM métabolisme des acides aminés
Chaine Youtube (abonnement). Plusieurs vidéos multilingues



- من علوم الحياة إلى البيوكيمياء
Des Sciences de la vie au Lycée à la Biochimie à l'Université

Congrès,
Conférences,...
- Congrès, Conférences
- Cours, Workshops
- Bourses, Postdocs
- Biotech-ecolo annonces
CONCOURS:
- Concours de Pharmacie
- تحميل ملفات في مواضيع البيوكيمياء
Téléchargement de fichiers en Biochimie
مجلة
إخبارية - Newsletter
Concentrations.Vidéos explicatives